�R��(�Ɖu�O���u�����uIg�v)
�u�R�́v�Ƃ�����E�B���X���̍R���Ɍ�������Ƃ�����������Ă��悤�ɂȂ������̂ŁA
�{���́u�Ɖu�O���u����(Immunoglobulin��Ig)�v�ƌĂ�܂��B
�q�g���͂��߂Ƃ��鐶�̓��ł́A�O������N�����Ă�������E�C���X�A�ԕ��y�ё̓��ɔ��ǂ����K���זE�Ȃǂٕ̈����A
�����ł͂Ȃ��u�ȁv�Ɣ��f���u�R���v�ƔF�����܂��B
�u�R�́v�́A�����S�Ăٕ̈����u�R���v�F�����Č������铭���������^���p�N���q�ŁA
�����p����B�זE�݂̂��Y�����邱�Ƃ��o������̂ł��B
B�זE������o���ꂽ�R�̂͊�{�I�ɂ͌��t���Ȃǂ����̗���ɏ���ĕ��V���Ă��܂����A
�Y�����ꂽ�����B�זE�\�ʂɋ��鎞�́u�R�����Z�v�^�[�v�Ƃ����āu�R���v��F������G�p��A�߂܂����
�Ƃ��đ��݂��Ă��܂��B
�q�g���͂��߂Ƃ������̂ɂƂ��āA�����̑̂ɐN�����Ă��������ȊO�̂��̂��ׂẮu�ȁv�ł���A
����͑��������ɂƂ��ĊQ���Ȃ����̂Ȃ̂ł��B
�Ⴆ�A�a�����������Ă���O157�Ȃǂ�����C���t���G���U�E�C���X�A
�ԕ��ǂȂǂ̃A�����M�[�������N�������˂Ȃ��ԕ��Ȃǂł��B
�����̔Ȃł���R�����E�ە������Ĕr�����悤�Ƃ���̂��u�Ɖu�����v�ƌĂ�A
���̖Ɖu�����ɓ����������̂��Ɖu�O���u�����܂��͍R�̂Ƃ������̂Ȃ̂ł��B
���H���͑̂̒��ɐN�����Ă��܂���u�ٕ��v�ł����Ă��Ɖu�����͋N���Ȃ��̂ł��B
�u�����튯�ƖƉu�v�̃y�[�W�ɂ��������ڂ��������Ă���܂��B
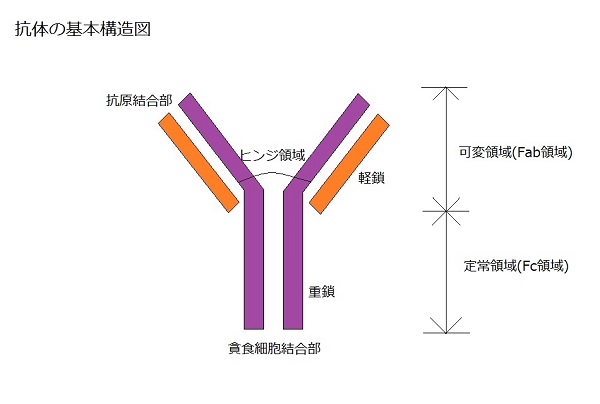
��������͏�L�́u�R�̂̊�{�\���}�v���Q�Ƃ��Ă��������B
�R�̂̊�{�\���̓A�~�m�_�Ƃ������q����R�W�܂����u�|���y�v�`�h���v�ŏo�����u�y���v�Ɓu�d���v��4�{��������Y���^���Ȃ��Ă��܂��B
�����āAY���̗��r�̕����Ɂu�y���v���ЂƂ��A�r����Y���̉��̖_�ɂ����Ă̕����Ɂu�d���v�����ł͕��s���āA
�r�̕����ł͕�����Ă��ꂼ��́u�y���v�ƕ��s���Ȃ���4�{���킹�ē�d��Y���^���`����Ă��܂��B
�}�ł͂킩�肸�炢�Ǝv���܂����A�傫�����d��(���q�ʂ�50,000�`77,000��)�̕����y��(���q��25,000��)�̔{�قǂ���܂��B
(�����ňꉞ�{���炢�ɂ��܂���)
������Y���^�̗��r�����镔�����u�q���W�̈�(������)�v�ƌĂсA���r�̕������u�ϗ̈�(Fab�̈�)�v���̕������u���̈�(Fc�̈�)�v�ƌĂ�ł��܂��B
�ϗ̈�͈ٕ���߂܂���ꏊ�ŁA���ɐ�[�̕����͑��l�ȍR���ɍ��킹�ăA�~�m�_�̔z��ɑ��l�ȕω��������܂��B
�����Ă݂�Α�R�̌����ɍ��킹�邽�߂ɑ�R�̌��������Ă���l�ȕ��ł����A
��̍R�͈̂��ނ̍R���ɑ��錮���������Ƃ��o���܂���A���Ƃ�������ނ̍R�̂ł��ϗ̈��[�̌��́A
���̐��̒�������E�B���X���̍R���ɍ��킹�ĕ�������ނ�����Ƃ������ɂȂ�܂��B
���A������
���������זE���}�N���t�@�[�W�̗l���ÐH�זE�B���A
�̓��ɐN�����Ă����ٕ��ł���u�R���v���E�ە������āu�R���v�����āA
���������T�זE��B�זE�ɂ��́u�R���v�ɍ��킹���u�R�́v�����Ɩ��߂��āA
���߂Ă�������E�B���X�̌����ɍ����������R�̂��ł���̂ŁA
���܂�ɂ�������������ɋ���Ƃ����Ƃ������ɂ͖��ɗ��R�̂��̓��ɖ����Ƃ������ɂȂ�܂��B
�q�g���������ł�����A�ߓx�ȎE�ۂ�R�ۂɂ͉������ɖ������o�Ă��܂��̂ŋC�����Ă��������B
��)
��ōR����T�זE���u�����v�Ə����܂������AT�זE�ɖڂ������ł͖����A
�����܂ł���g�I�ȕ\���ł��B
�ł��A�z���g�ɖڂ��݂����炻��͂���Ō��Ă݂����C�����܂��B
�֘A�y�[�W��
��
B�זE
�����튯�ƖƉu
����זE
�}�N���t�@�[�W
T�זE
����E�C���X�Ȃǂ͎���̕\�ʂ�(�q�g���̐���)�̍זE�̕\�ʂɌ��������邱�ƂŐN�����Ő��������̂����ʂł����A
�u���a��p�v�Ƃ����čזE�ɐN�������O�ɍR�̂��R���Ɍ������Ă��܂��A����E�C���X�̊����͂���߂���A
�őf�̓Ő������������邱�Ƃ��o���܂��B
�C���t���G���U�Ȃǂ̃E�C���X�ł͑���̍זE�ɐN�����邽�߂ɁA����̍זE�ɂ������Č݂��̊O�����m��Z��������
�����̃Q�m�����זE���ɓ���Ă��܂�(����)�h�����̂悤�Ȗ�ڂ�����AHA(�w�}�O���`�j���܂��̓w���A�O���`�j��:�Ԍ����ÏW�f)��
�Ă��R����������ς��������̕\�ʂɕ��������Ă��邽�߁A���̈��ɍR�̂͑勓���Č������悤�Ƃ��܂��B
�܂�(���⍩���A�ւȂǂ�)�őf�́A
�R�̂Ƃقڕ��q��(�傫��)���������炢�Ȃ̂�1�̓őf�ɂ�1�̍R�̂�������ƍl�����Ă��܂��B
�ϗ̈������E�C���X�Ȃǂ̍R���Ɍ�������ƁA�q���W�̈悪�ω����Ă��ꂪ�ڈ�ɂȂ�A
���R�Ɖu�n���}�N���t�@�[�W�┒�����Ȃǂ�����Ă��܂��B
���̈�ɂ́uFc��e�́v�ƌĂ���}�N���t�@�[�W�┒�����Ȃǂ��ÐH�זE�ƌ����o���镔��������A
��������Ɓu�I�u�\�j����(�܂��̓I�u�\�j����p)�v�Ƃ����āA�ÐH�זE�������ÐH��p�𑣐i��������ʂ�����܂��B
���ÐH�זE�͍R�̂��R���ƌ������Ă��邩��H�ׂ₷���ƌ�����ł��B�����A�R�̂��R���ƈꏏ�ɐH�ׂ��Ă��܂���ł����ǁc�c�����B
�܂��u��̊�������p�v�Ƃ����čR�̎��̂��R���ƌ�������ƍR�̂̋@�\��⊮����u��́v�ƌĂ��^���p�N�������������A
���炪�Ƃ炦�Ă���R���ƌ��������܂��B
����ƕ�̂́u�n�ہv�܂��́u�T�C�g���V�X�v�Ƃ��������̍זE����j�ĎE���Ă��܂����Ƃ��o���܂��B
���̕�̂ɂ��u�Ɖu�n�۔����v�����R�Ɖu���D������
�}�N���t�@�[�W���ÐH��p�Ɠ��l�ɁA
�����ڔj��Ƃ����Ɖu�n�ɂƂ��ďd�v�ȋ@�\�ƂȂ��Ă��܂��B
�����̍R�̂́A�q�g�̂��̂����ł��傫��������5���(IgG�AM�AA�AE�AD)�����݂��Ă��܂��B
�����ȖƉu����(���E�}�`�Ȃ�)
��ɐ���쓮���Ă���R�̂��Ɖu�@�\�Ȃ̂ł����A
�ԈႦ�Ă��܂����Ƃ�����܂��B
���i�́A�O������̍R��(����E�C���X�Ȃ�)������W�I�Ƃ��ĔF���A�U������̂ł����A
���̎��ȖƉu�����Ƃ����a�C�ɂȂ�Ɓu���ȁv�Ɓu�ȁv�̌����������Ȃ��Ȃ�A���Ȃ̍זE�܂ňٕ��Ƃ��ĔF���A�U�����邱�ƂɂȂ�܂��B
���q�g�ȊO�̍R��
��ɐҒœ����ő��݂��m�F����Ă��܂��B
�M���ނ̓q�g�Ɠ���IgG�AM�AA�AE�AD�����ł����A����ȊO(���ށA�����ށA���ނȂ�)�ł́AIgW�AX�AY����������悤�ł��B
����IgM�����͖Ɖu�O���u�����̍R�̂��������̒��ł͋��ʂɂ݂���悤�ł��B
�֘A�y�[�W��
��
���R�Ɖu
�}�N���t�@�[�W
�D����
�Ɖu
�uIgG�v(�Ɖu�O���u����G)
�����R�̂̑啔������(�q�g�̏ꍇ�Ɖu�O���u������70���ȏ�)���a��p�̔\�͂��ł������ƍl�����Ă��܂��B
Y���^��(�R�̂Ƃ��Ă�)�|�s�����[�Ȍ`(��L�́u�R�̂̊�{�\���}�v�̗l��)�����Ă��܂��B
�uIgM�v(�Ɖu�O���u����M)
�q�g�Ɖu�O���u������10�������߁AY���^�̊�{�`��5�~�`�Ɍ��������`���Ƃ��Ă��܂��B��Ɉ��ʂ������ɑ��݂��āA
B�זE�\�ʂɂ���Ƃ��͍ŏ��ɍR���̐N�������m����̂����̃^�C�v�ł��B
B�זE���R���ɐڐG�������ɁA�ŏ��ɎY�������R���ł�����܂��B
�֘A�y�[�W��
B�זE
�uIgA�v(�Ɖu�O���u����A)
�q�g�Ɖu�O���u������10���ȏ���߂Ă��܂��B���̈�̐�[(Y���^�̉��̖_�̒�)�ŁA
�������Ă����ʑ�IgA(pIgA)�ƒP�Ƃ̒P�ʑ�IgA(mIgA)�̓��ނ����݂��܂����P�ʑ̂̎��̋@�\�͗ǂ��������Ă��Ȃ��悤�ł����A
�������ł�mIgA�̕������|�I�ɑ����悤�ł��B
�����AIgA�̓����͓�ʑ̂�pIgA�̕��Ȃ̂ł��B
IgA�͔S����ŎY��(���t��S�t�A����A�A�ɑ���)�����ƁA
���זE�ŎY�����ꂽ����^���p�N���ƌ������ē�ʑ̂�pIgA�ɂȂ��ĔS�����זE����S�t�Ƌ��ɕ���(����^IgA�ƌ����܂�)����܂��B
�����ĊO����N�����Ă���R��(����E�C���X�Ȃ�)�ցA
������(�����A�@�o�A�A�H�S��)�Ȃǂ̔S����Ō������Ă��̊�����j�Q���Ă���̂ł��B
���ɁAB�זE�̖�60�`70�������z���Ă��钰�ǂł͌��t����IgG�ƁA
�S�����IgA�̓�d�\���̖h�q���C����~���ăq�g�̑̓��ōł����͂ƌ����Ă���u���ǖƉu�v�̏d�v�Ȉ�[���`�Â����Ă��܂��B
�֘A�y�[�W��
B�זE
�uIgD�v(�Ɖu�O���u����D)
���̓q�g�Ɖu�O���u������1�����x�ƌ����A�R�̂��Y������Ƃ���(�����n��)B�זE��IgM�����̎Y������A
���n����(IgM��)���ɕ\�o����̂�IgD�ł��B
���ׁ̈AB�זE�̐��n��R�̎Y���̗U���Ɋ֗^���Ă���ƍl�����Ă��܂��B
�֘A�y�[�W��
B�זE
�uIgE�v(�Ɖu�O���u����E)
�����q�g�Ɖu�O���u������0,001�����x�Ƌɒ[�ɏ��Ȃ��̂ł��B
�����ǂ̊��ɑ���Ɖu�Ɋ֗^���Ă���̂ł����A�t��IgE���u�얞�זE�v��u�D����v�ƌ������āA
�����̍זE���u�A�����Q��(�A�����M�[�������N��������)�v���������R���ƌ��������ꍇ�A
����(�A�����M�[����)�������N�������Ƃ��m���Ă��܂��B
���Ȃ݂ɂ��́AIgE��1966�N�ɓ��{�l�Ɖu�w�҂̐�����E�Ǝq���v�Ȃ��������܂����B
�Ɖu�͂����߂���ʂ�����T�v�������g�̂��Љ�����܂�
HABA�������@�u�r�t�B�Y�X�~�b�N�X150���v


�z������Ă���t�F�J���X��(�G���e���R�b�J�X���t�F�J���X��)�́A�v���o�C�I�e�B�N�X�Ƃ��Ă̐�����p�������Ă��鑼�ɂ��A
�R���X�e���[���⒆�����b�̒ቺ��p�A�A�����M�[���ᇁE���ȖƉu�����Ȃǂւ̉��p �����҂���Ă���V�^���_�ۂƂ��Ē��ڂ���Ă��܂��B
���ڂ����́A��L�̏��i�摜�����N��������T�C�g�ɓ��邩�A�܂��͉��L�̏ڍ׃y�[�W�ɂĂ��m�F���������B
�u�r�t�B�Y�X�~�b�N�X150���v�ڍ׃y�[�W��